Nutrition et pancréatite chronique
Pr D. RIGAUD - CHU Dijon
La pancréatite chronique est une maladie inflammatoire évoluant par poussées au cours desquelles la destruction des cellules acineuses et endocrines va à terme conduire au déficit exocrine (malabsorption) et endocrine (diabète). Dans la pancréatite chronique alcoolique, c’est la formation de bouchons protéiques secondairement calcifiés qui est responsable de ce processus. Ces bouchons obstruent les canaux excréteurs secondaires puis primaires du pancréas et vont induire douleurs, dilatation canalaire et faux kystes d’une part et destruction des acini et des îlots endocrines d’autre part (1,2). L’alimentation et la nutrition peuvent influencer l’évolution de la maladie de deux façons : elles participent à la genèse de l’affection, mais sont aussi modifiées par son cours.
En effet, le pancréas est un organe clé de l’absorption digestive des nutriments (protéines, lipides, glucides et vitamine B12 notamment). C’est aussi un organe déterminant dans l’utilisation du glucose par les cellules, grâce à la sécrétion d’insuline par les cellules béta des îlots de Langherhans. Le pancréas s’ouvre sur un carrefour stratégique, le duodénum, là où se mélangent 4 sécrétions exocrines (gastriques, biliaires, pancréatiques et duodénales). Ce carrefour est la première porte d’entrée des nutriments dans l’organisme, via la veine porte. C’est la raison pour laquelle un pancréas altéré induit de nombreuses perturbations digestives et métaboliques qui participent à une dégradation de l’état nutritionnel (1,2). Ainsi les relations entre nutrition et pancréatite chronique se déclinent-elles dans les 2 sens :
- L’alimentation et l’état nutritionnel, facteurs étiopathogéniques de la pancréatite chronique ;
- La malnutrition et l’assistance nutritive dans la pancréatite chronique.
Enfin, si l’alcool reste, notamment en France, la cause la plus fréquente de la pancréatite chronique (90 % des cas), il n’en résume pas l’étiologie. D’autres causes, comme la mucoviscidose, les anomalies canalaires congénitales, l’hyperparathyroïdie et la malnutrition protéo-énergétique sont bien reconnues.
1. De l'alimentation à la pancréatite chronique
1.1. L'alcool
Une consommation excessive d’alcool provoque une pancréatite chronique.
- Il n’y a pas de « dose seuil », contrairement à ce qui se passe pour la cirrhose,
- le risque de pancréatite chronique augmente de façon exponentielle avec la consommation d’alcool,
- l’effet de l’alcool sur le pancréas est cumulatif,
- le sexe a une influence nette sur le risque.
L’effet seuil : La quantité moyenne d’alcool pur à partir de laquelle le risque de pancréatite chronique augmente de façon significative dans la population pourrait être de 15 à 20 g/j chez la femme et de 20 à 30 g/j chez l’homme pendant au moins 10-15 ans (1,2,3). Donc, moins et moins longtemps que pour la cirrhose. Une question dès lors se pose, qui n’a pas reçu de réponse : pourquoi y a t-il moins de cas de pancréatite chronique que de cirrhose liées à l’alcool ?
|
Rappel : 1 litre de vin à 12° contient 120 mL, soit (120 x 0,8) = 96 g d’alcool pur puisque la densité de l’alcool est de 0,8 g/mL.
Ainsi : Une bouteille de vin « normale » (75 cL) contient 72 g d’alcool pur. Une bouteille de whisky (70 cL, 40°) contient 224 g d’alcool pur. |
|
Un « verre » pris au café du coin apporte environ 10 g d’alcool pur.
L’unité, au café, est en effet environ de 10 g d’alcool pur, qu’il s’agisse d’un ballon de rouge ou d’un gin tonic. « Un verre » = 10 g d’alcool pur est le chiffre retenu dans la littérature.
|
La toxicité de l’alcool sur le pancréas est cumulative : Comme pour tabac et cancer du poumon, comme pour alcool et cirrhose :
Le risque de pancréatite apparaîtrait vers la 10ème année, voire même plus tôt chez la femme. C’est donc environ 200 kg d’alcool pur en 15 ans qu’il faut consommer pour un homme (moitié moins chez une femme) pour voir augmenter le risque de pancréatite chronique, par rapport au risque encouru en cas d’absence de consommation. L’allure de la courbe d’augmentation du risque de pancréatite chronique en fonction de la consommation d’alcool est mal connue. Il double en 20 ans d’exposition au risque.
Enfin, à quantité d’alcool pur égale, le risque de survenue d’une pancréatite chronique ne dépend pas du type de boisson alcoolisée ingérée. Champagne ou gros rouge, bière ou cognac, ce qui compte, c’est la quantité d’alcool pur ingérée : ce n’est qu’une question de goût (et de prix de la pancréatite chronique) ! Ceci en fait semble bien opposer l’effet toxique des boissons alcoolisées sur le pancréas et l’effet protecteur de l’alcool sur les coronaires cardiaques.
L’influence du sexe : Homme et femme sont inégaux devant le risque. A quantité d’alcool pur égale, le risque de survenue d’une pancréatite chronique est deux fois plus élevé chez la femme que chez l’homme. La raison en est inconnue. On sait que le risque de survenue d’une pancréatite chronique varie en fonction des individus, pour des raisons mal comprises. Ces raisons seraient à la fois d’ordre génétique et alimentaire. Le sexe fait partie des facteurs génétiques.
1.2. Apports énergétiques et pancréatite chronique
Un point mérite réflexion : des apports nutritifs normaux protègent-ils de la pancréatite chronique ? En d’autres termes, la toxicité de l’alcool ne s’exprime-t-elle qu’en cas de déficits alimentaires et/ou de carences nutritionnelles.
En fait, en moyenne, les consommateurs d’alcool ne mangent pas moins que les autres (3). De plus, au stade de la pancréatite chronique compensée, avant les premières crises douloureuses, le malade atteint de pancréatite chronique alcoolique n’a pas une alimentation déséquilibrée (1,2) : les apports énergétiques non alcooliques, les apports protéiques, lipidiques et glucidiques du sujet alcoolique comme du malade porteur de pancréatite chronique « histologique » sont proches des apports recommandés et de ceux de la population générale.
![]() Résumons : « Manger bien », « boire en mangeant », « boire du bon vin » ne protègent pas de la pancréatite chronique !
Résumons : « Manger bien », « boire en mangeant », « boire du bon vin » ne protègent pas de la pancréatite chronique !
Mais les déficits alimentaires font le lit de la pancréatite chronique.
1.3. Apports protéiques et pancréatite chronique
Une opinion répandue mais fausse est que l’alcoolique, moins musclé que d’autres, mange moins de viande pour boire plus. Il n’en est rien : en Europe et en France, les apports protéiques de l’alcoolique et, à terme, de l’alcoolique atteint de pancréatite chronique en phase compensée, sont similaires à ceux d’une population de non buveurs ou d’ex-buveurs (2,3,4).
Mais il est probable en revanche que la dénutrition protéique majore le risque de pancréatite chronique ou en aggrave les conséquences.
2. De l'état nutritionnel à la pancréatite chronique
2.1. Malnutrition et pancréatite chronique
C’est la dénutrition protéo-énergétique qui est surtout responsable de pancréatite chronique. Un cas typique est la pancréatite chronique dite nutritionnelle observée dans les pays à bas niveau de vie et d’alimentation (décrite en Inde par exemple). La malnutrition y joue à l’évidence un rôle, mais d’autres facteurs y contribuent sûrement (contaminants alimentaires).
3. Retentissement nutritionnel de la pancréatite chronique
Le pancréas est un organe essentiel dans la digestion-absorption des macro-nutriments (protides, lipides, glucides) et dans la sécrétion d’hormones (insuline, glucagon, somatostatine, polypeptide pancréatique) dont deux sont clairement impliquées dans l’utilisation des hydrates de carbone. Il n’est donc pas étonnant que la pancréatite chronique, lorsqu’elle s’accompagne d’insuffisance pancréatique exocrine et endocrine, induise des perturbations de l’état nutritionnel.
3.1. Dénutrition et pancréatite chronique
L’amaigrissement et la dénutrition sont des complications fréquentes de la pancréatite chronique calcifiante alcoolique : les 2/3 environ des patients développeront une dénutrition au cours de l’évolution de la pancréatite.
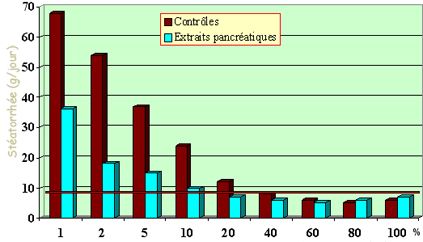
Cette dénutrition survient tard dans l’évolution de la pancréatite chronique. En effet, il est probable qu’il faut une destruction ou une amputation d’au moins 90 % de la glande pour qu’apparaissent des signes de malabsorption. Ainsi, il faut une perte d’environ 80 à 90 % de la sécrétion de lipase pour qu’apparaisse une stéatorrhée (Figure 1). Ceci est lié au fait que les activités enzymatiques digestives compensent longtemps le déficit pancréatique exocrine : lipase gastrique et intestinale, co-lipases, protéases duodéno-jéjunales et amylase salivaire notamment (1,5). De plus, la destruction de la queue du pancréas, là où se situe la majorité des îlots endocrines (et donc des réserves de sécrétion d’insuline), est tardive, expliquant la rareté du diabète dans les 15 premières années. Il n’en reste pas moins que c’est à l’occasion d’un diabète que l’on peut être amené à découvrir une pancréatite chronique.
Il s’agit d’une dénutrition protéo-énergétique, associant un déficit énergétique et un déficit azoté : il y a diminution des réserves énergétiques, c’est à dire fonte de la masse grasse et diminution des réserves protéiques, c’est à dire fonte de la masse maigre. La perte de poids des malades dénutris porte tout autant sur la masse grasse que sur la masse cellulaire maigre (c’est à dire la masse maigre totale moins l’eau extra-cellulaire ; Figure 1) : dans l’étude de Hébuterne et al, le déficit était de respectivement 34 % pour la masse grasse et 31 % pour la masse maigre (6). Ces déficits étaient semblables à ceux observés chez des malades dénutris n’ayant pas de pancréatite chronique.
Les mécanismes de cette dénutrition sont mal connus. Trois éléments y participent : la douleur, la malabsorption et le diabète.
La douleur : de façon continue, ou plus souvent au cours de poussées aiguës de la maladie, la douleur favorise la perte de poids par la peur de manger et l’anorexie qu’elle induit. Elle toucherait 60 à 90 % des malades.
La malabsorption : elle concerne de 25 à 45 % des malades. L’insuffisance pancréatique exocrine induit une maldigestion des graisses (lipases et colipases) et des vitamines liposolubles (A, D, E et K), des protéines, des glucides (peu parlante cliniquement), du calcium (par la formation de savons calciques avec les graisses et par carence en vitamine D) et de la vitamine B12 (par défaut de destruction par les enzymes protéolytiques pancréatiques du facteur R qui lie la vitamine B12 alimentaire et empêche sa liaison avec le facteur intrinsèque qui en permet l’absorption) (7,8). Enfin, la formation de savons calciques induit dans de rares cas une franche augmentation de l’absorption de l’oxalate ; l’hyperoxalurie qui en découle peut être responsable de la formation de calcul des voies excrétrices urinaires.
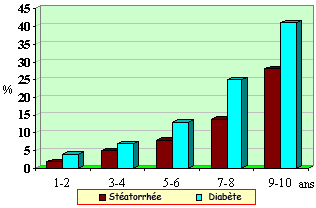
Le diabète : il s’agit d’un diabète insulinopénique. Sa fréquence augmente avec la durée d’évolution (Figure 2) : 10 à 15 % des malades ont un diabète dans les 5 premières années du diagnostic, contre 40 à 65 % après plus de 10 ans d’évolution (9). Il est associé plutôt à une hyperphagie qu’à une anorexie, au moins à sa phase initiale.
Quoi qu’il en soit, la malnutrition expose à une altération des fonctions immunitaires (notamment lorsqu’il y a un diabète) et des processus de régénération après destruction (faux kystes, nécrose pancréatique) ainsi qu’à une perte d’appétit qui renforce elle même la malnutrition.
3.2. Métabolisme et pancréatite chronique
3.2.1. Dépense énergétique de repos
La dépense énergétique de repos est un peu augmentée en cas de pancréatite chronique. Cette augmentation est fonction de la gravité de la pancréatite chronique, c’est à dire de son « activité » (nécrose et inflammation pancréatiques).
Hébuterne et al (6) ont mesuré la composition corporelle et la dépense énergétique de repos (DER) chez 33 malades atteints de pancréatite chronique calcifiante alcoolique. Les malades étaient séparés en 2 groupes : 20 malades étaient amaigris et 11 étaient de poids normal. La DER était plus élevée (de 17 %) dans le groupe de malades dénutris que dans le groupe de malades de poids normal, lorsque rapportée à la masse maigre. Elle était aussi plus élevée que celle de malades dénutris n’ayant pas de pancréatite chronique.
L’augmentation de la DER, lorsque rapportée à la masse maigre, suggère un hypermétabolisme. Celui-ci peut être lié à la consommation d’alcool et de tabac, mais surtout au syndrome inflammatoire qui accompagne les poussées de cette maladie chronique. Une augmentation de 15 % de la DER représente un surcroît non négligeable : à titre indicatif, chez un malade ayant des apports énergétiques similaires (et normaux à 2500 kcal/j), une telle augmentation sera responsable d’un déficit énergétique de 375 kcal/j, soit d’une perte de poids d’environ 50 g/j, et donc de la perte de 4 à 5 kg en 3 mois. Il est donc plausible que cette augmentation de la DER soit responsable, dans la pancréatite chronique calcifiante, de l’amaigrissement et de la dénutrition. Ceci mériterait d’être évalué par une étude longitudinale.
L’augmentation de la dépense énergétique de repos est plus nette en cas de pancréatite chronique associée à des signes d’activité qu’en cas de pancréatite chronique inactive. Cette augmentation pourrait être le fait d’une augmentation de la néoglucogénèse et d’une sécrétion accrue de cytokines.
3.2.2. Métabolisme des glucides
Le rôle du pancréas est essentiel dans le métabolisme des glucides (1,2,4).
En cas de pancréatite chronique, il n’est pas rare d’observer des épisodes d’hypoglycémie (potentialisés par l’alcool !) et des intolérances aux glucides. Le diabète est insulino-dépendant, expose au même complications dégénératives vasculaires que les autres formes de diabète (9) et s’avère de traitement difficile si l’on obtient pas le sevrage de l’alcool.
3.2.3. Métabolisme des lipides
La malabsorption des graisses est l’une des conséquences les plus saillantes de la pancréatite chronique (Figure 1). Une stéatorrhée est observée chez plus des 2/3 des malades au cours de l’évolution de la maladie. Elle est le fait des maladies évoluées, puisqu’une amputation de 90 % de la fonction pancréatique exocrine est nécessaire à l’apparition d’une stéatorrhée (5). Une stéatorrhée importante, supérieure à 20-25 g/j touche 10 % des malades atteints de pancréatite chronique alcoolique et 60% des enfants atteints de mucoviscidose. Avec la stéatorrhée, lorsqu’elle est importante, on observe une malabsorption des vitamines liposolubles, les vitamines A, D, E et K. Les déficits cliniques en vitamines A, E et K sont rares (5 % des cas), alors que l’ostéomalacie et l’ostéoporose liées au déficit en calcium et en vitamine D active sont fréquents (la moitié des malades). Ceci pourrait être le fait d’un déficit associé de synthèse de vitamine D3 par le foie en cas d’alcoolisme et de cirrhose associée.
En cas de pancréatite chronique, l’hypocholestérolémie est assez fréquente. Elle est en rapport avec la dénutrition. Une hypertriglycéridémie modérée n’est pas rare. Le rôle de l’alcool ne doit pas y être oublié !
3.2.4. Métabolisme des protides
Il est altéré par 2 facteurs : la malabsorption des protéines liée au déficit exocrine et l’état inflammatoire chronique en rapport avec les poussées de nécrose qui caractérisent la maladie. En revanche, pendant assez longtemps, il n’y a pas de carence protéique alimentaire vraie. A long terme, la carence d’apport énergétique global, le déficit d’absorption digestive des protéines et l’excès de catabolisme protéique vont favoriser la négativité chronique du bilan azoté. Il en découlera une diminution de la masse maigre et de la masse musculaire. Une fois soustraite l’eau extra-cellulaire, la perte de masse maigre est de l’ordre de 30 %. Cette perte de masse maigre est associée à une diminution de l’albuminémie et des autres marqueurs protéiques hépatiques de l’état nutritionnel, telles que pré-albumine ou transferrine.
Il y a donc intérêt à renforcer l’apport protéique, ou tout au moins à s’assurer que l’apport protéique est suffisant (> 1,4 g/kg poids/j).
4. Pancréatique chronique : Quel traitement ?
4.1. Faut-il arrêter l'alcool ?
| Il n’est pas parfaitement démontré, contrairement à ce qui se passe en cas de cirrhose, que l’arrêt de l’alcool s’accompagne d’une régression des anomalies histologiques et surtout des manifestations cliniques de la pancréatite chronique, avec réduction du degré de nécrose et de l’extension de la fibrose, et diminution de l’insuffisance exocrine et endocrine. |
Ainsi, les études portant sur l’évolution de la douleur et des poussées aiguës de la maladie à l’arrêt de l’alcool sont contradictoires. De même, il n’est pas démontré que l’on puisse retarder la survenue du diabète ou diminuer la stéatorrhée. Ceci est lié au fait que beaucoup de malades sont vus pour la première fois à un stade où plus de 90 % de la glande est détruite.
Cependant, il est probable que l’arrêt de l’alcool, dans une maladie qui évolue sur de longues années, permet d’en diminuer l’aggravation et donc peut-être d’accroître l’espérance de vie des malades atteints de pancréatite chronique.
4.2. Alimentation et pancréatite chronique
L’alimentation n’est le plus souvent pas altérée avant l’apparition des signes de gravité (malabsorption patente, diabète, hypertension portale, ictère). Cependant, un petit nombre de malades ont à ce stade des apports énergétiques et surtout protéiques insuffisants qu’il importe de compenser (2,4). Il en est ainsi notamment des malades qui sont dans des conditions sociales précaires.
En revanche, lorsque les signes de gravité sont installés, il n’est pas rare d’observer des signes de dénutrition. Il est plausible que la dénutrition aggrave l’insuffisance pancréatique. Ceci est particulièrement vrai en cas de pancréatite chronique compliquée d’hépatite ou de cirrhose alcoolique, c’est à dire chez 5 % des malades. Globalement, la dénutrition est plus rare en cas de pancréatite chronique alcoolique qu’en cas de mucoviscidose ou de pancréatite « tropicale ».
|
Un certain nombre de facteurs de risque de dénutrition et de carences multiples en micro-nutriments peuvent être dégagés :
|
En cas de malabsorption : Au stade de pancréatite évoluée, la stéatorrhée et la créatorrhée doivent être prises en compte dans l’évaluation des entrées énergétiques : le déficit énergétique entrant est de 9 kcal/g pour les graisses et de 4 kcal/g pour les protides ; la déperdition fécale de protéines est de 6,25 x azote (voir cas clinique). Une malabsorption nette doit faire prescrire une dose adéquate d’extraits pancréatiques pour diminuer les pertes énergétiques fécales et les pertes en vitamines liposolubles. Il n’y a, sauf cas de diabète, pas d’indication à restreindre la part des matières grasses dans l’alimentation : il suffit d’ajuster la dose d’extraits pancréatiques, y compris dans la mucoviscidose. En cas de malabsorption lipidique majeure (< 40 g/j), il est utile de remplacer une partie des matières grasses ajoutées par des triglycérides à chaîne moyenne (MCT), sans dépasser la dose de 20 à 30 g/j, pour des raisons de tolérance.
En cas de prise d’extraits pancréatiques, il faut déconseiller un régime trop riche en fibres : les fibres alimentaires, solubles et insolubles, captent et adsorbent les enzymes pancréatiques et s’opposent de ce fait à leur action. La pancréatite chronique est bien le seul cas où il n’est pas souhaitable d’augmenter les apports de fibres alimentaires.
En cas de diabète : L’existence d’un diabète change quelque peu la prise en charge du malade : c’est un facteur de mauvais pronostic ; il complique la prise en charge nutritionnelle, d’autant plus que l’insuffisance endocrine est le plus souvent associée à une insuffisance exocrine sévère (9). La pancréatite chronique représente 0,5 % des cas de diabète dans la population générale, 2 à 5 % dans la population alcoolique et 10 % des diabètes en pays tropical. La fréquence du diabète dans la pancréatite chronique croît avec la durée d’évolution de la pancréatite chronique calcifiante. Une pancréatectomie, surtout lorsqu’elle inclut la queue du pancréas, en augmente le risque de survenue. Le diabète de la pancréatite chronique peut s’accompagner d’un déficit en glucagon (l’hormone est sécrétée par les cellules alpha des îlots de Langherhans). Ce déficit favorise, en cas d’insulinothérapie, en particulier chez l’alcoolique, des épisodes d’hypoglycémie plus fréquents (25 % des cas) et plus profonds que dans le diabète de type 1 « classique » (9). C’est dire l’importance d’un régime équilibré, sans alcool, résolument riche en énergie (45 kcal/kg poids/j), en glucides (55 % des apports énergétiques), en protéines (15 à 18 %, ou 1,5 à 1,7 g/kg/j) et sans excès de lipides (30 à 33 % des apports énergétiques, soit 1,2 à 1,5 g/kg/j). Les lipides en excès, en effet, majorent la stéatorrhée et peuvent modifier la cinétique d’absorption des glucides. Le régime sera basé par 3 repas par jour et une collation. Si ces règles simples sont respectées, les besoins en insuline ne semblent pas plus important que dans le diabète de type 1 « classique ». On peut par ailleurs tout à fait appliquer à ces patients les régimes d’insulinothérapie intensive. Contrairement à une opinion répandue, la neuropathie périphérique, les complications rénales et neurologiques ne semblent pas plus rares, à durée du diabète équivalente, que dans le diabète de type 1. Les facteurs individuels (alcool, facteurs génétiques) jouent, ici comme ailleurs, un rôle non négligeable. La fréquence de survenue des complications dégénératives du diabète rend nécessaire, ici comme dans le diabète de type 1, un contrôle optimal de la glycémie à jeun et postprandiale.
4.3. Carences en micro-nutriments et pancréatite chronique
4.3.1. Vitamines
Des carences patentes en vitamines B12, A, D, E et K ont été décrites en cas de pancréatite chronique (7,8). Elles sont en fait rares : moins de 5 % des patients développent un tableau clinique de carence en vitamine B12, A, E et K.
Cependant, des déficits chroniques en calcium et vitamine D avec ostéomalacie et ostéoporose peuvent se constituer chez 20 % des malades. Une supplémentation systématique en vitamine D est donc souhaitable.
4.3.2. Minéraux et oligo-éléments
Fer : Une carence martiale est rare en cas de pancréatite chronique (2). Elle est liée à un saignement digestif : anti-inflammatoires non stéroïdiens ou gastropathie d’hypertension portale.
A l’inverse, un excès de fer sérique est noté chez 10 % des malades atteints de pancréatite chronique alcoolique.
Calcium : La densité osseuse en calcium et les stocks minéraux et protéiques osseux sont diminués en cas de pancréatite chronique. Carence d’apport en calcium, déficit d’absorption digestive du calcium et de la vitamine D, voire défaut de synthèse hépatique en vitamine 25 (OH) D3 en sont responsables.
Zinc : La sécrétion pancréatique contient un ligand du zinc, qui en favorise l’absorption. Une diminution de la concentration plasmatique de zinc a été rapportée en cas de pancréatite chronique alcoolique et non alcoolique.
Magnésium : quelques malades alcooliques se plaignent de crampes et faiblesses musculaires qui cèdent à une supplémentation en magnésium. Il s’agit de patients stéatorrhéiques et le plus souvent dénutris ou diabétiques (2).
4.4. Assistance Nutritive et pancréatite chronique
| Il n’est pas clairement démontré qu’une assistance nutritionnelle diminue la morbidité et la mortalité en cas de poussée aiguë modérée de pancréatite chronique. En cas de poussée aiguë grave associée à une dénutrition moyenne ou sévère, la mortalité est inversement corrélée au catabolisme azoté. Il est donc logique de proposer une assistance nutritive chez ces malades. On ignore en revanche si l’assistance nutritive permet de diminuer morbidité et mortalité en cas d’intervention chirurgicale pancréatique. |
En pratique que proposer : En cas de poussée aiguë de pancréatite chronique, il faut assurer un apport d’azote et d’énergie adéquat, tenant compte de l’hypercatabolisme et du déficit nutritionnel, à savoir :
- 1,4 g protéines/kg poids /j et de 40 kcal/kg poids /j en l’absence de déficit
- et de l’ordre de 1,8 g protéines/kg poids /j et de 55 à 60 kcal/kg poids /j en cas de déficit nutritionnel.
La décision d’une assistance nutritive en cas de poussée aiguë de pancréatite chronique repose sur l’évaluation stricte de l’état nutritionnel et la longueur attendue du jeûne imposé par les douleurs. Si ce dernier risque de durer plus de 4 à 6 jours et si le malade est dénutri, il faut entreprendre une assistance nutritive. Celle-ci doit plutôt être une nutrition entérale à débit continu qu’une nutrition parentérale, dont les risques infectieux sont plus grands, en cas de pancréatite aiguë (10,11). En cas de pancréatite aiguë grave, Kalfarentzos et al (11) ont démontré que la nutrition entérale par sonde naso-jéjunale était mieux tolérée, entraînait moins de complications et était moins chère que la nutrition parentérale. On sait maintenant par ailleurs qu’il n’y a pas lieu de réduire l’apport lipidique et que l’utilisation des triglycérides à chaîne moyenne est utile seulement en cas de déficit important de la sécrétion pancréatique. Chez ces malades graves, il serait souhaitable, en cas de nutrition parentérale, d’apporter de la glutamine (0,4 à 0,5 g/kg/j), que les solutés standards ne contiennent pas.
Evaluer l’état nutritionnel : Les éléments ci-dessus montrent qu’il faut évaluer régulièrement l’état nutritionnel. La décision d’une assistance nutritive, en dehors des poussées, repose sur cette évaluation. A cet égard, l’importance de l’anorexie, des troubles digestifs et de la réduction des ingesta, un état fébrile, une perte de poids rapide sont autant d’arguments en faveur de la mise en route d’une assistance nutritive. Celle-ci devient obligatoire si une pancréatectomie étendue est décidée.
La mesure de la composition corporelle est essentielle. La fonte du pli cutané tricipital et surtout la fonte des masses musculaires, l’existence d’atteinte des phanères (peau desquamante, perlèche, ongles striés et cassants, cheveux secs et fragiles) ainsi que l’hypoalbuminémie et l’hypopréalbuminémie permettent de diagnostiquer une dénutrition.
|
On peut faire les propositions suivantes :
|
![]() En conclusion
En conclusion
Les relations entre nutrition et pancréatite chronique se font dans les 2 sens. L’alcool tient ici une place majeure. Il convient d’obtenir le sevrage, en prévenant le malade que le bénéfice immédiat (sur les douleurs, la stéatorrhée, le diabète) ne sera pas évident. Le développement d’un diabète vrai constitue un facteur de mauvais pronostic qui va aussi compliquer la prise en charge, surtout chez le malade alcoolique. En cas de pancréatite chronique, il faut régulièrement évaluer l’état nutritionnel. Si la dénutrition est évidente et si les apports énergétiques sont effondrés, il faut recourir à une assistance nutritive. Il s’agira plutôt alors d’une nutrition entérale.
5. Bibliographie
- Grendell JH. Nutrition and absorption in disease of the pancreas. Clinics in gastroenterology 1983 ; 12 : 551-563.
- Scuro LA, Vantini I. Nutritional problems and support in chronic pancreatitis. In « Nutrition in Gastrointestinal diseases ». Ed. Barbara L ; Raven Press (New Jork) 1987 : 273-83.
- Rueff B. « Alcoologie clinique ». Ed. Flammarion Médecine Science (Paris) 1989.
- Sarles H. An international survey on nutrition in pancreatitis. Digestion 1973 ; 9 : 389-403.
- DiMagno EP, Go VLH, Summerskill WHJ. Relations between pancreatic enzyme output and malabsorption in severe pancreatic insufficiency. N Engl J Med 1973 ; 288 : 813-5..
- Hébuterne X, Hastier P, Péroux JL, Zeboudj N, Delmont JP, Rampal P. Resting energy expenditure in patients with alcoholic chronic pancreatitis. Dig Dis Science, 1996 ; 41 : 533-9.
- Dutta SK, Bustin MP, Russell RM, Costa BS. Deficiency of fat soluble vitamins in treated patients with pancreatic insufficiency. Ann Intern Med 1982 ; 97 : 549-52.
- Sontag SJ, Spencer H, Norris C, Osis D. Studies on mineral and trace element metabolism in exocrine pancreatic insufficiency. Gastroenterology 1984 ; 86 : 1261A.
- Del Prato S, Tiengo A. Pancreatic diabetes. Diabetes Reviews 1993 ; 1 : 260-285.
- Zazzo JF. Nutrition entérale versus parentérale au cours des pancréatites aiguës. Nutr Clin Métab 1994 ; 8 : 249-54.
- Kalfarentzos F, Kehagias J, Mead N. Enteral nutrition is superior to parenteral nutrition in severe acute pancreatitis : results of a randomized trial. Br J Surg 1997 ; 84 : 1665-9.
|
Nutriment |
Anomalie, conséquences | Remarques |
| Dépense énergétique |
accrue |
Y compris quand rapportée à la masse maigre active |
| Glucides |
n Intolérance aux HC |
Liée à l’insuffisance pancréatique endocrine |
|
|
|
|
| Lipides |
n Hypocholestérolémie |
Dénutrition |
| Protéines |
* Hypoprotidémie portant sur protéines |
Catabolisme accru et synthèse diminuée |
| Fer |
* Stocks élevés |
Rôle de l’alcool |
|
|
|
|
| Vitamines A, D, E et K |
Insuffisance exocrine et malabsorption lipidique |
Rôle de l’alcool |
|
Vitamines B1, B2, B6 et B12 |
surtout vit B6 |
Rôle de l’alcool, facteur R |
|
Calcium |
Ostéoporose |
Rôle de l’alcool, de la stéatorrhée (savons calciques) |
|
Zinc |
déficit immunitaire, altération de goût et de l’odorat |
Rôle de l’alcool ? |
|
Magnésium |
crampes musculaires |
Rares |