Traitement de l'anorexie mentale par nutrition entérale de complément : suivi à 12 mois
RIGAUD D, POUPARD AT, BOULIER A, MIGNON M
Présenté par le Professeur Daniel RIGAUD
Professeur de Nutrition, Université de Bourgogne
Étude réalisée dans le service de Gastroentérologie et Nutrition du CHU Bichat-Claude Bernard, 75877 Paris Cedex 18.
| Résumé de l'étude : |
| L'anorexie mentale est une maladie chronique caractérisée par la peur de prendre du poids et de devenir obèse. Malgré l'extrême dénutrition dans laquelle se trouvent nombre de ces malades et la mortalité qui en découle (10 % de décès après 15 ans d'évolution), l'intérêt d'une assistance nutritive par voie entérale n'a jamais été évaluée. Le but de la présente étude était d'évaluer l'efficacité d'une nutrition entérale discontinue d'appoint sur l'évolution à court et moyen terme (un an) chez 281 malades atteints soit d'une forme restrictive soit d'une forme boulimique de l'affection. Chez 61 d'entre eux, une étude prospective avec tirage au sort, en ouvert, était réalisée. Deux groupes étaient comparés : 31 malades reçurent une alimentation orale ad libitum et une nutrition entérale discontinue d'appoint tandis que les 30 autres ne furent traités que par réalimentation par voie orale. Dans les 2 groupes, une prise en charge psychothérapeutique et diététique était assurée. |
| Notre étude, qui est la première étude prospective longitudinale avec tirage au sort dans l'anorexie mentale, a mis en évidence que la nutrition entérale discontinue d'appoint, associée à la réalimentation per os, offrait certains avantages sur une approche fondée sur la seule alimentation per os. Les malades prenaient du poids plus vite, ne mangeaient pas moins, diversifiaient autant leur alimentation et amélioraient de la même façon leur comportement alimentaire. L'hospitalisation, pour un même gain de poids (fixé au départ) était ainsi plus courte. Il se pourrait même que la prise de poids soit de meilleure qualité, puisque la prise d'eau dans le secteur eau extracellulaire était un peu (non significativement) moins grande dans le groupe " nutrition entérale " que dans le groupe contrôle. |
| Un autre avantage encore semble exister pour les malades atteint(e)s de boulimies et/ou de vomissements : la nutrition entérale discontinue permet d'obtenir plus facilement et plus souvent la réduction ou l'arrêt des crises de boulimie et/ou des vomissements. |
| Il est clair enfin que la nutrition entérale ne se conçoit chez ces malades que parfaitement articulée avec une approche psychothérapeutique associant thérapie cognitive et comportementale, groupe de soutien et de relaxation et prise en charge au long court, de plusieurs années. |
1. Traitement de l'anorexie mentale par nutrition entérale de complément : suivi à 12 mois
L'anorexie mentale est une maladie chronique caractérisée par la peur de prendre du poids et de devenir obèse et par la dénutrition, parfois extrême, qui en découle (1,11,12). La perte de poids est constante (elle fait partie des critères diagnostiques de la maladie).
Il s'agit d'une maladie touchant des sujets jeunes, en règle des femmes (90 à 95 % des cas) et dont le devenir à court et long terme est conditionné avant tout par le risque vital lié à la dénutrition et aux vomissements, lorsqu'ils existent (19,23,26,28,29, 31-35). En effet, ces facteurs altèrent les capacités musculaires, et en particulier celles des muscles lisses, du diaphragme et des autres muscles respiratoires et du myocarde (23,26,28,29, 32-34)
Il existe en effet deux formes d'anorexie mentale (6,16,18,19,35,36) : l'anorexie mentale restrictive pure, où aucune autre manœuvre de perte de poids que la restriction alimentaire n'est employée ; la forme avec vomissements et/ou crises de boulimie, où les vomissements et la boulimie ajoutent aux risques liés à la dénutrition leurs éléments de gravité propres (hypokaliémie, alcalose métabolique, potomanie et hyponatrémie, insuffisance rénale…).
Curieusement, alors même que la dénutrition est extrêmement fréquente et qu'elle est responsable de plus des ¾ des cas d'une mortalité qui touche des femmes jeunes (8 à 15 % de décès à 10-15 ans, à un âge moyen de 30-35 ans), aucune étude prospective n'a cherché à étudier l'intérêt de la nutrition entérale discontinue de complément ou exclusive dans l'anorexie mentale. Quelques rares publications en font état (2,4,9,17,21). Certains auteurs réputés dans le traitement de l'anorexie ne l'évoquent même pas (5,14,18-20,27,36,39,41).
Cet état de fait est probablement lié au fait que l'anorexie mentale est une maladie traitée par des psychiatres peu formés aux techniques de renutrition. Ceci explique au demeurant que la nutrition entérale ait mauvaise presse dans cette maladie. Elle est volontiers accusée d'être un frein à la réalimentation et à la thérapie comportementale. Les malades sous nutrition entérale discontinue de complément auraient plus de mal à se réalimenter par voie orale et à travailler sur leur comportement alimentaire. Au mieux, ces malades enclins à tricher et à refuser de prendre du poids feraient tout pour faire échouer la nutrition entérale discontinue de complément : refus initial ou retrait de la sonde nasogastrique, refus ou jet des flacons de mélanges nutritifs.
Le but du présent travail était de montrer que ces assertions représentent une position de principe ne reposant sur aucune preuve scientifique. Nous voulions apprécier l'acceptabilité d'une nutrition entérale discontinue de complément, sa faisabilité, ses incidents et accidents et les résultats nutritionnels et comportementaux à court (pendant l'hospitalisation) et moyen terme (évaluation 6 et 12 mois après arrêt de la nutrition entérale discontinue de complément).
Il s'agit d'un travail portant sur 281 malades atteints d'anorexie mentale hospitalisés dans un même service spécialisé dans la prise en charge des troubles du comportement alimentaire. La période d'étude est de 12 ans. Parmi ces malades, 61 malades ont été inclus dans une étude prospective, entre 1996 et 1999, et tirés au sort pour avoir soit une réalimentation exclusivement per os, soit une réalimentation orale associée à une nutrition entérale discontinue de complément. A la même époque (1996-99), 89 malades étaient hospitalisés dans l'Unité de Nutrition : 11 ont refusé de participer (6 d'entre eux ont souhaité avoir la sonde nasogastrique d'emblé), 13 étaient trop dénutris (indice de masse corporelle < 12 kg/(m)2) pour être tirés au sort et 4 autres n'étaient hospitalisés que pour un temps court avant de retourner dans le Service psychiatrique qui les avait adressés.
1.1. Patients et méthodes
Patients
Les malades répondaient tous aux critères de l'anorexie mentale tels que définis par le DSM IV et Feighner (1,11,12) : perte d'au moins 15 % de leur poids (ou poids inférieur à 85 % du poids minimum pour l'âge et la taille) ; peur de grossir et de devenir obèse ; distorsion du comportement alimentaire ; refus de maintenir ou d'atteindre un poids minimal normal ; absence d'autre affection somatique ou mentale ; deux des signes suivants : aménorrhée (96 %) ; hyperactivité physique (86 %), boulimie ou vomissements (33 %), bradycardie (fréquence cardiaque < 50 puls/min : 68 %), âge inférieur à 25 ans au début de l'affection (98 %).
Certaines des caractéristiques des malades sont indiquées dans le tableau I. Comme toujours, la plupart étaient de sexe féminin. Concernant les 76 patients qui avaient une forme avec vomissements et/ou crises de boulimie, la crise de boulimie était définie comme l'ingestion en un temps court d'une quantité importante d'aliments, sans sélection, sans sensation de faim ni de plaisir, s'accompagnant d'une sensation de perte de contrôle, de culpabilité et de tentatives répétées de limiter les effets des crises (ou d'accroître l'amaigrissement) en utilisant vomissements et/ou laxatifs. Il devait y avoir ou y avoir eu au moins 3 crises par semaine pendant au moins 6 mois. Les patients avec vomissements sans boulimie ont été inclus dans ce sous-groupe car ils partagent le même pronostic et la même évolution à long terme (apparition de crises de boulimie lors ou après la période de renutrition dans près de la moitié des cas).
|
Population "rétrospective"
(n = 220) |
Population tirée au sort
(n = 61) |
|||
| Restrictives (n=144) |
Boulimiques* (n=76) |
Restrictives (n=43) |
Boulimiques* (n=18) |
|
| Femmes (%) | 94 % | 96 % | 98 % | 95 % |
| Ages (ans) | 21 ± 3,6 | 25,1 ± 4,7 $ | 22,5 ± 4,5 | 24,2 ± 3,8 $ |
| Poids (kg) | 33,2 ± 4,6 | 36,1 ± 6,2 | 34,0 ± 3,9 | 37,7 ± 4,3 |
| IMC (kg/(m)²) actuel | 12,7 ± 1,8 | 13,8 ± 2,4 | 12,1 ± 1,5 | 13,2 ± 2,0 |
| Perte de poids (kg) | 20,4 ± 4,1 | 14,8 ± 6,3 | 18,6 ± 2,5 | 16,7 ± 4,9 |
| Durée d'évolution (médiane) | 5 ± 2 ans | 4,7 ± 3 ans | 4,5 ± 1,9 ans | 3,2 ± 2 ans |
| N° de crises (/semaines)* | 0 | 18 ± 5 | 0 | 13 ± 6 |
| Nombre d'hospitalisations antérieures (extrêmes) | 1 à 5 | 1 à 4 | 1 à 4 | 1 à 3 |
| IMC (kg/(m)²) avant la maladie | 21,7 ± 1,4 | 20,1 ± 2,2 | 24,8 ± 3,1 | 21,1 ± 1,9 |
IMC : Indice de masse corporelle
* Nombre de crises de boulimie ou de vomissements par semaine
$ P < 0,05 vs forme restrictive
Tous les malades avaient une maladie sévère : durée d'évolution longue (de plus de 6 ans dans 2/3 des cas), échecs thérapeutiques en ambulatoire (91 % des cas), rechute(s) ou récidive(s) précoces après une ou des hospitalisations antérieures (88 % des cas), importance de la perte de poids et/ou des angoisses autour du poids et de l'alimentation (73 % des cas), vomissements et/ou crises de boulimie pluri-quotidiens (33 % des cas), indice de masse corporelle (IMC) actuel très bas (voir tableau I).
Méthodes
Lors de l'admission, le malade était informé du mode de prise en charge dans le service. Cette dernière y repose depuis 15 ans sur une triple approche : nutritionnelle, psychothérapeutique et comportementale. L'équipe définit avec le malade les 4 objectifs : 1) obtenir un poids minimum normal (IMC > 18,5 kg/(m)2), 2) atteindre et maintenir des apports énergétiques et en nutriments conformes à ses besoins lorsqu'il(elle) pèsera le poids défini comme objectif, 3) retrouver un comportement alimentaire plus acceptable, 4) travailler sur les caractéristiques psychiques qui ont permis à la maladie de s'installer.
Tout au long de l'hospitalisation le malade bénéficie également d'une psychothérapie de soutien pour lutter contre dépression et angoisse.
Pour les besoins de l'étude, les malades étaient informés que pour atteindre le premier objectif (un poids normal bas : IMC > 18,5 kg/(m)2), une nutrition entérale discontinue d'appoint par sonde nasogastrique leur serait proposée, après tirage au sort.
Les 10 intérêts de cette nutrition entérale discontinue d'appoint leur étaient expliqués : elle préserve les fonctions vitales tant que le malade est dans un état grave ; elle apporte le minimum d'énergie nécessaire au fonctionnement de l'organisme ; elle assure l'apport en vitamines et minéraux que l'alimentation très réduite actuelle ne permet pas ; elle offre, du fait de la sonde gastrique, un barrage " mécanique " aux vomissements ; elle supprime l'état de jeûne chronique qui renforce le besoin des crises de boulimie ; elle donne au patient, vis à vis de sa famille et d'elle-même, un statut de malade ; elle lui permet d'éviter la remise en cause des parents face à leur échec ; elle donne au malade le temps de travailler efficacement et en profondeur sur son alimentation et son comportement alimentaire sans avoir à " manger 3000 calories ", notamment lorsque, boulimique, la suralimentation lui fait peur (à juste titre !) ; elle assure une coercition minimale qui permet d'éviter le plus souvent le recours à l'isolement (les visites, le téléphone et les permissions sont autorisés de principe dès que l'état physique le permet).
Lors des 3 à 5 premiers jours, étaient évalués les aspects suivants (3, 10, 15, 16, 18, 19, 30, 31, 35) : les apports alimentaires (variété, quantité), le comportement alimentaire (Eating disorder inventory, Eating attitude scale, nombre de vomissements et/ou de crises de boulimie), les apports énergétiques (calories, protides, lipides, glucides et micronutriments selon le logiciel BILNUT), l'état mental (indice de Beck évaluant notamment l'état dépressif), l'état nutritionnel (clinique, biologique), la composition corporelle (anthropométrie, impédancemétrie) et la dépense énergétique de repos (calorimétrie indirecte).
Au 4ème-6ème jour, en cas de consentement informé du malade, la nutrition entérale discontinue d'appoint était ou non débutée. Le malade était tiré au sort pour recevoir soit la totalité des apports par l'alimentation, soit le complément par sonde.
Si le malade était tiré au sort pour le groupe " nutrition entérale discontinue d'appoint ", la sonde était mise en place et sa position vérifiée cliniquement et radiologiquement. La quantité de mélange nutritif polymérique standard (Nutrison®, Normoréal® ou Entérogyl® selon les marchés) était fixée au cas par cas et expliquée au malade. L'apport énergétique entéral était déterminé en fonction de plusieurs critères : l'état nutritionnel (en cas d'IMC < 11 kg/(m)2, la renutrition était initiée à un niveau égal à la dépense énergétique de repos) ; la progression des apports alimentaires. En bref, l'attitude était la suivante : on fixait avec la malade l'objectif pondéral et le temps approximatif pour l'obtenir. Ceci permettait de définir un gain de poids quotidien souhaité (le plus souvent entre 150 et 250 g/j). En fonction de la dépense énergétique de repos (DER) mesurée et d'un facteur permettant de prendre en compte l'activité physique (le plus souvent 1,5 fois la DER), le niveau des apports énergétiques et protéiques totaux de maintenance était fixé. Le coût énergétique du gain de poids était fixé, en fonction des études antérieures, à 7,5 kcal/g, soit par exemple un total de 850 kcal (DER) x 1,5 + (150 g x 7,5 kcal/g) = 1275 + 1125 = 2400 kcal/j. Ce total était expliqué à la malade. Ceci participait des premières séances de travail de thérapie comportementale. Dès lors, il était convenu avec le patient que plus il mangerait, plus l'apport par mélange nutritif diminuerait, en sorte que le total reste constant (2400 kcal/j dans l'exemple ci-dessus).
Le débit et les horaires de la nutrition entérale étaient décidés en accord avec le malade et l'équipe soignante. Si la malade était dans le groupe " renutrition per os ", aucun supplément diététique n'était prescrit.
L'alimentation et la nutrition entérale discontinue d'appoint étaient limitées en NaCl (régime sans sel systématique dès l'entrée) pour éviter la prise d'œdème quasi constante et participer à la lutte contre la peur de manger et les crises de boulimie (liées au désir excessif de se " faire plaisir "). Le régime normosodé (environ 8 à 10 g de NaCl) était prescrit lorsqu'un IMC de 15 kg/(m)2 était atteint. La prescription de vitamines, de minéraux et d'oligoéléments était faite au cas par cas. En règle, en dessous d'un IMC de 15 kg/(m)2, les malades recevaient, per os ou par sonde selon le groupe, un flacon de Nonan®, 500 mg de calcium, 10 µg de vitamine D3 et 1 ou 2 comprimés de polyvitamines.
Lors de l'hospitalisation et du suivi, les traitements antidépresseurs, sédatifs et thymoanaleptiques étaient à l'appréciation du thérapeute. Ils n'étaient en aucun cas systématiquement prescrits.
1.2. Critères d'évaluation de l'interêt de la nutrition entérale discontinue d'appoint
Différents critères ont été utilisés pour évaluer l'efficacité de la nutrition entérale discontinue d'appoint sur l'évolution de la maladie (3,10,15,16,18,19,30,31,35).
1.2.1. Critères nutritionnels
Poids, IMC, composition corporelle par anthropométrie et impédancemétrie à double fréquence avec mesure de la masse maigre (MM), de la masse musculaire (circonférence brachiale, créatininurie/24 h sur 3 jours), de la masse grasse (MG), de l'eau totale (ET) et de l'eau extra- et intracellulaire (EEC et EIC) ; évaluation de la dénutrition sur des critères cliniques (peau et phanères, langue, oedèmes des membres inférieurs, force musculaire par dynamomètre manuel...) et biologiques (albumine, transthyrétine, transferrine, hémoglobine, numération formule sanguine, bilan phosphocalcique et magnésium, zinc sanguin et urinaire…) ; évaluation des vomissements (parotidose, élévation des ALAT et ASAT, hypokaliémie, hypochlorémie, hypercréatininémie, alcalose métabolique).
La mesure de la composition corporelle et de la dépense énergétique par calorimétrie indirecte était effectuée en moyenne toutes les 2 semaines (3,24,30).
1.2.2. Critères alimentaires
Évolution des ingesta, par interrogatoire alimentaire quotidien effectué par une diététicienne rompue à la prise en charge des troubles du comportement alimentaire (25-31). Après recueil des données alimentaires (repas et collations évalués par recueil effectué par la malade sous contrôle du personnel soignant), les aliments et quantités étaient entrés dans un logiciel de traitement des valeurs nutritionnelles pour ordinateur PC (BILNUT). Le suivi des apports de la nutrition entérale était effectué par contrôle de la quantité restante et estimation de ce qui avait été perfusé auprès de la malade et des infirmières.
1.2.3. Critères comportementaux
Ont été pris en compte : peur de grossir et de manger ; résistance à la prise de poids ; évolution de la variété de l'alimentation ; nombre de vomissements et/ou de crises de boulimie ; et aussi degré de l'état dépressif, de la nervosité, des angoisses et de l'hyperactivité physique. Pour ces variables, un questionnaire était remis au malade indiquant " un peu ", " plutôt peu ", " moyennement ", " beaucoup ", " énormément ", " pas du tout ". Ex. : " Avez-vous des vomissements ? " : réponse " plutôt peu " ; " Vous sentez-vous angoissée ? " : réponse " énormément ".
1.2.4. Critères de tolérance
Nombre de sondes nasogastriques posées durant la renutrition, incidents et accidents (reflux gastro-oesophagien, vomissements, sinusite, pneumopathies, obstruction ou saignements nasaux) ; un questionnaire assez long était par ailleurs remis au malade en début de la nutrition entérale pour évaluer ce que représentait pour lui(elle) la nutrition entérale et la sonde à l'instant présent (voir annexe). A titre indicatif : la sonde (les malades emploient ce terme pour désigner la nutrition entérale) représente-t elle pour vous actuellement : un frein à manger ; un frein vis à vis de la prise de poids ; une peur ; une sécurité ? …
1.2.5. Critères économiques
Durée de l'hospitalisation ; coût de la nutrition entérale ; prescriptions annexes (antidépresseurs).
1.2.6. Critères de suivi
Évolution du poids et des ingesta au retrait de la sonde, à 3 mois et à 6 mois ; pourcentage de malades en rechute (amaigrissement, renforcement des peurs et angoisses autour du poids et de l'alimentation, restriction alimentaire, reprise des vomissements et/ou crises de boulimie), durée de la période sans rechute, pourcentage de malades rehospitalisés.
1.3. Résultats étude prospective (61 patients)
1.3.1. Poids et composition corporelle
L'évolution du poids et de la composition corporelle sont indiqués dans la Figure 1. On voit que la prise de poids était plus rapide dans le groupe " nutrition entérale discontinue d'appoint " (P < 0,02). La prise de masse maigre et de masse grasse aussi (P < 0,03).
En revanche, il n'existait pas de différence mesurable entre les 2 groupes en ce qui concernait le gain différentiel de masse maigre et grasse : à la fin de l'hospitalisation, chez les malades des 2 groupes, la prise de poids s'était répartie également entre masse maigre et masse grasse : 61,4 % de masse maigre et 38,6 % de masse grasse.
La prise d'eau dans le secteur extracellulaire était plus grande dans le groupe contrôle que dans le groupe thérapeutique, mais la différence n'était pas significative.
Figure 1 : Évolution du poids et de la composition corporelle dans le groupe "nutrition entérale" et dans le groupe contrôle
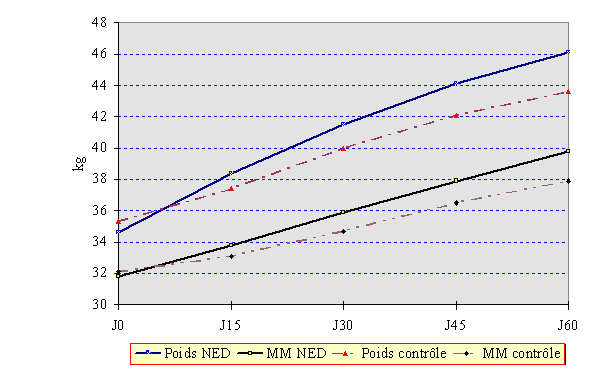
NED : nutrition entérale discontinue ; MM : masse maigre ; " contrôle " : groupe contrôle
J0 à J60 : depuis le jour précédent la NED jusqu'au 60ème jour de NED.
1.3.2. Apports énergétiques
L'augmentation des apports énergétiques per os au fil du temps n'était pas significativement différente entre les 2 groupes (Tableau II), ni pour l'apport global ni pour les protides, lipides et glucides.
942 ± 175
(n = 31)
(n = 30)
Restrictives
(n=22) Boulimiques*
(n=9) Restrictives
(n=21) Boulimiques*
(n=9)
Femmes (%)
95 %
100 %
100 %
89 %
Energie (kcal/j) à J0
Energie à 15 jours
Energie à 1 mois
Energie à 2 mois
850 ± 124
1712 ± 213
1983 ± 185
2008 ± 1941234 ± 321
1621 ± 297
1822 ± 312
1799 ± 268
1826 ± 251
2077 ± 233
2015 ± 2181098 ± 279
1745 ± 197
1909 ± 240
2122 ± 386
Lipides (g/j) à J0
Lipides (g/j) à 1 mois
Lipides (g/j) à 2 mois 31 ± 2
76 ± 7
71 ± 939 ± 8
67 ± 9
66 ± 1133 ± 4
61 ± 6
69 ± 635 ± 6
71 ± 8
70 ± 8
Glucides (g/j) à J0
Glucides (g/j) à 1 mois
Glucides (g/j) à 2 mois 106 ± 27
252 ± 36
267 ± 43188 ± 34
226 ± 39
245 ± 32117 ± 21
254 ± 41
251 ± 48171 ± 23
232 ± 37
254 ± 29
Protides (g/j) à J0
Protides (g/j) à 1 mois
Protides (g/j) à 2 mois 36 ± 7
71 ± 7
75 ± 933 ± 9
78 ± 12
56 ± 1144 ± 6
82 ± 6
97 ± 824 ± 5
69 ± 5
83 ± 4
* Apports en énergie et macronutriments : hors crises
L'augmentation des apports en énergie, lipides, glucides et protides de J0 à 1 mois était significative dans les 2 groupes
(P < 0,01), sans différence entre eux.
Il existait une différence significative entre boulimiques et restrictives concernant l'apport énergétique (P<0,05)
et glucidique (P<0,03) à J0.
En d'autres termes, l'apport énergétique global (per os plus entéral) était significativement plus important dans le groupe " nutrition entérale discontinue d'appoint " que dans le groupe contrôle (P < 0,001).
Fait important, l'arrêt de la nutrition entérale discontinue d'appoint ne s'accompagnait pas d'une réduction des apports énergétiques (Tableau II). Au contraire, 20 des 31 malades (64 %) compensèrent efficacement la réduction des apports par mélanges nutritifs par une augmentation de même ampleur de leur ingesta. Ceci se faisait progressivement, conformément au projet élaboré avec le malade.
La diversification alimentaire était obtenue de la même façon dans les 2 groupes, avec un avantage modéré pour le groupe " nutrition entérale discontinue d'appoint " (Tableau III).
11 ± 6
(n = 31)
(n = 30)
Restrictives
(n=22) Boulimiques*
(n=9) Restrictives
(n=21) Boulimiques*
(n=9)
N° aliments introduits**
à 1 semaine
à 2 semaines
à 1 mois
à 2 mois12 ± 4
26 ± 5
38 ± 13
41 ± 719 ± 7
34 ± 8
44 ± 10
49 ± 11
23 ± 7
34 ± 9
39 ± 1015 ± 9
32 ± 11
46 ± 12
55 ± 13
Matières grasses ajoutées (en g/j)
à 1 semaine
à 2 semaines
à 1 mois
à 2 mois 3,8 ± 1,6
16,5 ± 3,4
15,2 ± 3,7
18,5 ± 3,44,5 ± 2,3
11,8 ± 2,7
18,2 ± 2,2
17,6 ± 2,93,1 ± 1,9
15,1 ± 2,6
16,9 ± 2,4
16,5 ± 3,14,4 ± 1,8
12,5 ± 2,1
15,1 ± 3,2
14,8 ± 3,2
Saccharose ajouté (en g/j)
à 1 semaine
à 2 semaines
à 1 mois
à 2 mois 0,5 ± 0,8
4,6 ± 2,3
14,2 ± 3,7
18,9 ± 4,35,0 ± 1,2
7,1 ± 2,3
18,0 ± 2,8
16,8 ± 3,90,8 ± 1,0
5,4 ± 1,6
11,7 ± 1,8
17,5 ± 3,43,2 ± 1,1
9,7 ± 2,5
14,3 ± 2,9
21,6 ± 4,3
** valeurs cumulées
De même, l'arrêt des crises de boulimie et/ou des vomissements était obtenu plus souvent et plus rapidement dans le groupe " nutrition entérale discontinue d'appoint " (Figure 2 ; P < 0,01).
FIGURE 2 : Évolution des apports énergétiques dans le groupe " nutrition entérale " et dans le groupe contrôle
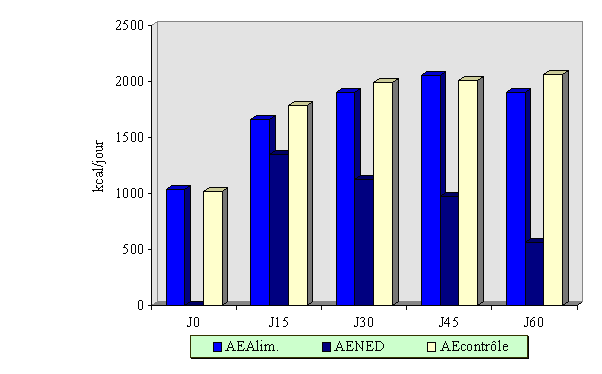
On voit que les apports énergétiques per os étaient sensiblement les mêmes dans les 2 groupes.
De ce fait, les apports liés à la NED font toute la différence d'apports entre les 2 groupes.
L'évolution du comportement alimentaire ne différait pas entre les 2 groupes : le comportement s'améliorait de la même façon. A la fin de l'hospitalisation, 54 % de ces malades graves pouvaient être considérés comme exempts de l'ensemble des signes cardinaux de l'anorexie : peur de manger, peur de grossir, peur de ne pas pouvoir s'arrêter de prendre du poids, refus ou angoisse à maintenir le poids obtenu, trouble de l'image corporelle. Concernant ce dernier point et à titre d'exemple, 48 des 61 malades (78 %) se jugeaient très maigres dès la 3ème semaine d'hospitalisation.
A la question " vous sentez-vous angoissée à l'idée d'atteindre l'objectif de poids fixé ? (IMC = 18,5 kg/(m)2) ", la réponse à l'admission dans le service était " énormément " chez 27 des 61 malades (44, contre 15 (24,5 %) après un mois de prise en charge (7 sur 31 dans le groupe " nutrition entérale discontinue d'appoint ", 8 sur 30 dans le groupe contrôle).
1.3.3. Critères de tolérance
2,3 ± 0,9 sondes nasogastriques (médiane : 1,94 ; extrêmes : 1 à 8) ont été posées durant une renutrition de 58 ± 11 jours en moyenne. Il y a eu peu d'incidents et accidents : 3 reflux gastro-oesophagiens importants obligeant à la prescription d'inhibiteurs de la pompe à protons gastrique, 3 cas de sinusite traitée par antibiotiques, 1 pneumopathie infectieuse, 2 obstructions avec saignements nasaux ayant obligé à changer la sonde de narine.
Les réponses à certaines des questions issues du questionnaire sont indiquées dans le tableau IV. Ce qui se dégageait, c'est que la nutrition entérale discontinue d'appoint faisait plutôt peur lors de sa pose, mais qu'ensuite, elle était de mieux en mieux supportée, car elle offrait aux malades des vrais choix de lutte contre leur maladie. Un point important est la réponse à la question qui concerne les malades vomisseuses : " la sonde vous aide-t-elle à limiter vos vomissements ? " : 8 des 10 malades répondaient " énormément ". A titre indicatif, la sonde, après un mois de nutrition entérale discontinue d'appoint, représentait une sécurité et une aide pour respectivement 87 % et 68 % des malades. Pour 18 d'entre eux (58 %), la sonde n'était ni un frein à manger, ni un frein vis à vis de la prise de poids. A l'inverse, pour 5 malades (16 %), la sonde freinait considérablement leur appétit et leur prise de poids ; A l'arrêt de la nutrition entérale discontinue d'appoint, 4 de ces 5 malades ont maigri, parce qu'ils mangeaient moins encore que lorsque la sonde était en place. Le dernier malade a effectivement mangé plus.
|
Groupe NED
(n = 31) |
||
| Restrictives (n=22) |
Boulimiques* (n=9) |
|
| La redoutent fortement | ||
| à 1 semaine à 2 semaines à 1 mois à 2 mois |
18 (82%) 14 12 7 (32%) |
4 (44%) 3 1 1 |
| Trouvent en elle une aide | ||
| à 1 semaine à 2 semaines à 1 mois à 2 mois |
3 (13%) 5 15 17 (77%) |
4 (44%) 6 7 7 (78%) |
| Pensent qu'elle est en frein | ||
| à 1 semaine à 2 semaines à 1 mois à 2 mois |
21 (95%) 14 9 4 (18%) |
8 (89%) 3 1 1 (11%) |
1.3.4. Critères économiques
La durée d'hospitalisation était significativement plus courte en cas de nutrition entérale discontinue d'appoint que dans le groupe contrôle : 74 ±12 jours versus 87 ± 10 jours. Le coût de la nutrition entérale était raisonnable : 1868 ± 124 F. Les prescriptions médicamenteuses annexes (antidépresseurs, anxiolytiques, sédatifs) étaient un peu plus fréquentes dans le groupe " nutrition entérale discontinue d'appoint " que dans le groupe contrôle : 8 des 31 malades du groupe " sonde " contre 5 des 30 malades de l'autre groupe (NS).
1.3.5. Critères de suivi
L'évolution du poids et des ingesta, tant au retrait de la sonde qu'à 3 mois, 6 mois et 1 an, ne différait pas d'un groupe à l'autre (Tableau V).
|
Groupe NED
(n = 31) |
Groupe contrôle
(n = 30) |
|||
| Restrictives (n=22) |
Boulimiques* (n=9) |
Restrictives (n=21) |
Boulimiques* (n=9) |
|
| Poids (kg) à Jfin | 45,4 ± 2,5 44,7 ± 2,1 43,8 ± 2,6 |
47,5 ± 1,9 48,9 ± 2,5 46,2 ± 2,9 |
42,8 ± 2,0 |
44,7 ± 2,7 43,6 ± 2,9 42,8 ± 2,6 |
| Energie (kcal/j) à Jfin Energie à 3 mois Energie à 12 mois |
2008 ± 194 1871 ± 221 1704 ± 185 |
1799 ± 268 1921 ± 235 1819 ± 255 |
2015 ± 218 1836 ± 204 1703 ± 278 |
2122 ± 386 1790 ± 223 1881 ± 257 |
| Lipides (g/j) à Jfin Lipides (g/j) à 3 mois Lipides (g/j) à 12 mois |
71 ± 9 65 ± 8 54 ± 8 |
66 ± 11 69 ± 10 63 ± 9 |
69 ± 6 63 ± 7 59 ± 5 |
70 ± 8 62 ± 10 69 ± 11 |
| Glucides (g/j) à Jfin Glucides (g/j) à 3 mois Glucides (g/j) à 12 mois |
267 ± 43 250 ± 42 237 ± 38 |
245 ± 32 252 ± 31 249 ± 38 |
251 ± 48 245 ± 40 222 ± 35 |
254 ± 29 242 ± 57 248 ± 36 |
| Protides (g/j) à Jfin Protides (g/j) à 3 mois Protides (g/j) à 12 mois |
75 ± 9 69 ± 7 67 ± 10 |
56 ± 11 73 ± 10 64 ± 9 |
97 ± 8 72 ± 9 71 ± 8 |
83 ± 4 66 ± 8 67 ± 12 |
Il n'y avait de différence entre les 2 groupes pour aucune de ces variables.
De même, l'évolution du poids était sensiblement la même, même si le poids restait plus élevé dans le groupe " nutrition entérale discontinue d'appoint " que dans le groupe contrôle.
Le pourcentage de malades ayant rechuté à 1 an (amaigrissement, renforcement des peurs et angoisses autour du poids et de l'alimentation, restriction alimentaire, reprise des vomissements et/ou crises de boulimie) était identique dans les 2 groupes : 13 sur 31 dans le groupe " nutrition entérale discontinue d'appoint " et 16 sur 30 dans l'autre.
La durée de la période sans rechute était plus grande dans le groupe " nutrition entérale discontinue d'appoint " que dans l'autre : 34,3 ± 8,2 semaines vs 26,8 ± 7,5 semaines dans le groupe contrôle (P < 0,05).
Le pourcentage de malades réhospitalisés ne différait pas entre les 2 groupes : 4 sur 31 contre 6 sur 30 (NS).
1.4. Résultats : étude rétrospective (220 patients)
L'analyse des 220 dossiers des malades hospitalisés en 12 ans dans le Service du fait de troubles du comportement alimentaire et mis sous nutrition entérale discontinue d'appoint pour plus d'un mois permet de dégager les faits suivants :
1.4.1. Poids et composition corporelle
L'évolution du poids et de la composition corporelle ont été les suivants : prise de poids : 178 ± 17 g/j (1,24 kg/semaine) ; prise de masse maigre : 100 ± 14 g/j (56 % du poids pris) ; prise de masse grasse : 78 ± 24 g/j (44 %).
Une tendance à la rétention hydro-sodée a été observée chez 82 % des malades (n = 162) ayant un IMC < 15 kg/(m)2 (soit 198 des 220 patients). Elle se traduisait par des oedèmes dans 29 % des cas (n = 57) avant renutrition, par l'existence ou l'augmentation sous renutrition de l'eau extracellulaire et de l'eau totale (avec un rapport eau extra- sur eau intracellulaire supérieur à 1,0), une augmentation ou l'apparition d'œdèmes des membres inférieurs malgré le régime hyposodé dans 35 % des cas (n = 69), une inversion de rapport Na+/K+ urinaire ou une excrétion urinaire de sodium < 20 mmol/24 h dans 159 cas (3 patientes utilisaient des diurétiques).
Au delà d'un IMC < 15 kg/(m)2, une correction de la rétention hydro-sodée était notée dans 91 % des cas (147 des 162 malades) : la courbe d'évolution de l'eau extracellulaire et de l'eau totale s'infléchissait (l'eau extracellulaire restait stable, tandis que la masse maigre sèche et la masse grasse suivait la même courbe qu'avant). Ceci est la raison pour laquelle, malgré des apports énergétiques moyens maintenus au dessus de leurs besoins énergétiques de maintenance, certaines de ces patientes arrêtent de prendre du poids pendant une semaine à 10 jours au passage de l'IMC de 15 kg/(m)2. : la perte d'eau, dont témoigne l'augmentation de l'excrétion urinaire de sodium, " compense " l'augmentation de la masse " sèche ". Il faut donc être prudent, avant de les accuser de mensonge ou dissimulation de nourriture.
1.4.2. Apports énergétiques
L'augmentation des apports énergétiques per os au fil du temps était significative (P < 0,001) : 854 ± 371 kcal/j à l'admission, 1239 ± 478 kcal/j après une semaine de nutrition entérale discontinue d'appoint, 1416 ± 324 kcal/j après 2 semaines, 1765 ± 396 kcal/j après un mois, 1747 ± 255 kcal/j après 2 mois, 1813 ± 287 kcal/j à l'arrêt de la nutrition entérale discontinue d'appoint et 2118 ± 216 kcal/j à la sortie de l'hôpital.
Cette augmentation portait sur les protides et les glucides, mais aussi sur les lipides : l'apport lipidique passait de 32 ± 5 g/j à l'admission à 64 ± 12 g/j à un mois, 67 ± 15 g/j à 2 mois, 64 ± 12 g/j à l'arrêt de la nutrition et à 74 ± 9 g/j à la sortie (P < 0,001).
Fait important, l'arrêt de la nutrition entérale discontinue d'appoint ne s'accompagnait pas d'une réduction des apports énergétiques ni lipidiques. Au contraire, 72 % des patients compensaient efficacement la réduction des apports entéraux par une augmentation de même ampleur de leur ingesta et notamment des matières grasses alimentaires. Ceci se faisait conformément au projet élaboré avec le malade.
1.4.3. Comportement alimentaire
La diversification alimentaire était le plus souvent obtenue pendant la durée de la nutrition entérale discontinue d'appoint : 86 % des malades (n = 189) introduisaient au moins 20 aliments nouveaux après un mois de renutrition.
L'arrêt des crises de boulimie et/ou des vomissements était observé dans 72 % des cas.
L'évolution du comportement alimentaire était favorable dans plus de 4/5 des cas : réduction de la peur de manger dans 62 % des cas ; réduction de la peur de grossir dans 69 % des cas. Néanmoins, environ un malade sur deux (48 %) gardait des angoisses notables vis à vis de l'avenir et de son poids corporel (peur d'être incapable de les maîtriser après la sortie).
A la fin de l'hospitalisation, 58 % des malades semblaient exempts des signes cardinaux de l'anorexie. A titre indicatif, 206 des 220 malades (93 %) se jugeaient très maigres dès la 3ème semaine d'hospitalisation (contre seulement 11 % à l'admission, soit une franche diminution du trouble de l'image corporelle).
Parmi les 205 malades ayant répondu à la question " Vous sentez-vous angoissée à l'idée d'atteindre l'objectif de poids fixé ? (IMC = 18,5 kg/(m)2) ", la réponse à l'admission dans le service était " énormément " chez 197 malades (96 %) et seulement chez 102 malades (49 %) après un mois de prise en charge.
1.4.4. Critères de tolérance
2,7 ± 1,2 sondes nasogastriques (médiane : 1,7 ; extrêmes : 1 à 6) ont été posées durant une renutrition de 54 ± 17 jours en moyenne. Il y a eu peu d'incidents et accidents : 11 malades (5 %) ont eu un reflux gastro-oesophagien important obligeant à la prescription d'antisécrétoires gastriques, 13 patientes (6 %) ont eu une sinusite aiguë cédant sous antibiotiques, 1 de celles-ci a eu une pneumopathie infectieuse, 8 obstructions avec saignements nasaux ont obligé à changer la sonde de narine. Enfin, 15 malades (7 %) n'ont pas pu supporter psychologiquement la nutrition entérale et ont retiré à plusieurs reprises la sonde, si bien que l'arrêt de la nutrition entérale discontinue d'appoint a été décidé.
La nutrition entérale discontinue d'appoint était un objet de forte crainte et de rejet au début dans 57 % des cas (125 malades). Par la suite, elle était de mieux en mieux acceptée. Durant la phase de renutrition, 18 malades (8 %) ont affirmé que la sonde freinait considérablement leur appétit et leur prise de poids. A l'arrêt de la nutrition entérale discontinue d'appoint, 14 de ces 18 malades ont remaigri, dont 11 reconnurent que c'était parce qu'ils mangeaient moins encore que lors de la période de nutrition entérale.
1.4.5. Critères économiques
La durée de la nutrition entérale discontinue d'appoint était de 54 ± 17 jours. La durée de l'hospitalisation était de 68 ± 13 jours.
Il y eut des prescriptions médicamenteuses annexes (antidépresseurs, anxiolytiques, sédatifs) chez 142 malades (64 %). Il n'y avait pas de différence statistique de prise de poids ou d'apport énergétique entre les malades sous et les malades sans antidépresseurs ou anxiolytiques.
1.4.6. Critères de suivi
L'évolution du poids et des apports énergétiques après sortie de l'hôpital est indiquée dans le tableau VI.
| Restrictives (n=22) | Boulimiques* (n=9) | |
| Poids (kg) à Jfin Poids (kg) à 3 mois Poids (kg) à 12 mois |
47,2 ± 2,8 45,4 ± 2,9 44,6 ± 2,1 |
49,1 ± 2,4 47,8 ± 2,7 46,9 ± 2,5 |
| Energie (kcal/j) à Jfin Energie à 3 mois Energie à 12 mois |
2118 ± 216 1861 ± 243 1659 ± 175 |
1945 ± 252 1821 ± 214 1777 ± 213 |
| Lipides (g/j) à Jfin Lipides (g/j) à 3 mois Lipides (g/j) à 12 mois |
75 ± 9 68 ± 6 62 ± 10 |
73 ± 8 69 ± 9 61 ± 10 |
| Glucides (g/j) à Jfin Glucides (g/j) à 3 mois Glucides (g/j) à 12 mois |
284 ± 48 251 ± 45 217 ± 48 |
253 ± 41 238 ± 51 243 ± 36 |
| Protides (g/j) à Jfin Protides (g/j) à 3 mois Protides (g/j) à 12 mois |
75 ± 9 61 ± 5 58 ± 8 |
69 ± 13 62 ± 9 64 ± 10 |
L'évolution se fait vers une lente dégradation de l'état nutritionnel et des apports énergétiques.
Le pourcentage de malades ayant rechuté à 1 an (amaigrissement, renforcement des peurs et angoisses autour du poids et de l'alimentation, restriction alimentaire, reprise des vomissements et/ou crises de boulimie) était de 42 % (n = 88 sur 209 patients pour lesquels des données ont pu être recueillies). La durée de la période sans rechute chez les malades ayant rechuté était de 24,5 ± 10,4 semaines.
Le pourcentage de malades réhospitalisés dans l'année était de 27 % (58 des 216 malades qui ont pu être contactés ou suivis pendant au moins un an).
1.5. Discussion
La présente étude est la première étude prospective longitudinale avec tirage au sort visant à démontrer l'intérêt de la nutrition entérale dans le traitement à court terme de l'anorexie mentale. Elle met en évidence que la nutrition entérale discontinue d'appoint, associée à la réalimentation per os, offre quelques avantages sur une approche fondée sur la seule alimentation per os. Les malades prennent du poids plus vite, ne mangent pas moins, diversifient autant leur alimentation et améliorent de la même façon leur comportement alimentaire. L'hospitalisation, pour un même gain de poids (fixé au départ) peut être ainsi plus courte. Il se pourrait même que la prise de poids soit de meilleure qualité, puisque la prise d'eau dans le secteur eau extracellulaire était un peu (non significativement) moins grande.
Un avantage plus important encore semble exister pour les malades atteint(e)s de boulimies et/ou de vomissements. En effet, la nutrition entérale discontinue d'appoint permet d'obtenir plus facilement et plus souvent la réduction ou l'arrêt des crises. Ceci pourrait être lié au fait que le mélange nutritif perfusé assure un débit plus constant de nutriments énergétiques au fil de la journée, limite les hypoglycémies et s'oppose ainsi efficacement aux mécanismes métaboliques de la crise de boulimie. De plus, la sonde en place offre (aux dires des malades) un " barrage " mécanique ou psychologique efficace aux vomissements, sans doute par la peur qu'ont les patients de " vomir " la sonde ou plus probablement par l'aide qu'elles sentent que l'équipe médicale leur apporte.
Il serait abusif d'affirmer que la nutrition entérale discontinue d'appoint est un traitement de fond de l'anorexie mentale qui en permet la guérison. Mais, même dans des maladies comme la maladie de Crohn, où la nutrition entérale peut prétendre à un effet thérapeutique " physiopathologique ", son efficacité à moyen terme sur le cours de l'affection n'a pu être démontrée. L'anorexie mentale est une maladie à deux composantes, une nutritionnelle et une psychologique, et la nutrition artificielle, quelle qu'elle soit, ne peut pas prétendre à une action thérapeutique sur ce deuxième aspect.
En revanche, la nutrition entérale discontinue d'appoint permet de passer un cap et d'assurer sans risque la survie des malades gravement dénutris en attendant qu'ils puissent lutter plus efficacement contre leur trouble du comportement alimentaire. Il n'y a pas de raison que le médecin, bien que ne sachant pas traiter le trouble du comportement, néglige l'aspect nutritionnel, puisque le plus souvent c'est de dénutrition que meurent les patients.
Il est intéressant par ailleurs de constater que la nutrition entérale discontinue d'appoint ne s'oppose d'aucune façon au travail de fond sur le comportement alimentaire. Au contraire. Il est, à notre point de vue, essentiel de posséder une technique qui permette au malade d'atteindre à son rythme et de défendre des apports énergétiques par les repas qui soient proches de ceux qui seront les siens lorsqu'il sera sorti de l'hôpital. En effet, la nutrition entérale " apportant le complément ", le patient peut se consacrer au travail nécessaire à mettre sur pied, avec le diététicien, une alimentation semblable à celle qu'il aura lorsqu'il aura atteint le poids fixé comme objectif et dont la teneur calorique a été estimée individuellement en fonction de la dépense énergétique de repos et de l'importance de l'activité physique du malade.
Enfin, l'effet de cette technique de renutrition sur l'évolution du poids, des ingesta et du comportement alimentaire est plutôt positif, puisque plus d'une fois sur deux, un maintien du résultat obtenu peut être maintenu au moins un an, ce qui permet de classer cette approche parmi les meilleures existantes actuellement.
De nombreux points très importants doivent être soulignés pour que la nutrition entérale discontinue d'appoint soit utilisée au mieux par les équipes soignantes :
Un soin particulier doit être apporté aux explications données aux malades : celles-ci bien sûr doivent être données à tout malade, mais plus particulièrement à des malades angoissés à l'idée de prendre du poids. Il faut leur expliquer que la nutrition entérale discontinue d'appoint n'est pas un objet là pour les " gaver ", mais bien pour les aider à lutter personnellement contre leur trouble du comportement alimentaire. Les points abordés plus haut doivent être détaillés.
La bonne position de la sonde dans la partie basse de l'estomac (qui est nettement sous-ombilicale chez ces malades dénutris) doit être vérifiée régulièrement (et par un cliché radiologique au moindre doute). Il s'agit en effet de sujets dénutris dont les capacités de vidange gastrique et la fonction anti-reflux du sphincter inférieur de l'œsophage sont altérées. La réalité de la perfusion du mélange nutritif doit être constamment contrôlée, afin d'évaluer avec précision le niveau des apports énergétiques réels. Ceci doit être fait atant pour des raisons métaboliques (risques inhérents à une réalimentation trop intensive chez les malades très dénutris) que psychologiques (pour ne pas mettre tout le monde dans une situation de dissimulation).
Le débit de la nutrition entérale discontinue d'appoint est fonction de la gravité de la dénutrition (IMC < 12 kg/(m)2) et des souhaits de la malade : un compromis doit être trouvé entre les nécessités métaboliques (débit < 2,5 mL/min) et le souhait des malades (débit le plus rapide possible !).
Le niveau d'apport énergétique par la nutrition entérale discontinue d'appoint doit être fonction des apports oraux : le niveau global est fixé avec le patient et celui de la nutrition entérale sera fonction des apports per os : plus ceux-ci augmentent, plus ceux de la nutrition entérale doivent être diminués.
La nutrition entérale discontinue d'appoint doit être arrêtée dès que la malade a atteint par sa seule alimentation le niveau d'apport énergétique calculé comme étant celui qui sera nécessaire pour stabiliser le poids défini comme objectif. La nutrition entérale doit naturellement être reprise si les repas deviennent insuffisants.
L'accompagnement est essentiel dans une affection où il y a de tels blocages psychologiques face à la peur de manger et de grossir : le soutien par un psychothérapeute, des séances de thérapie comportementale et, idéalement, des groupes thérapeutiques de soutien (groupe de parole, d'expression corporelle et émotionnelle, groupe de relaxation).
1.6. Bibliographie
 American Psychiatric Association. Diagnostic and statistical manual of mental disorder; 4th ed. Washington DC: American Psychiatric Association 1994
American Psychiatric Association. Diagnostic and statistical manual of mental disorder; 4th ed. Washington DC: American Psychiatric Association 1994- Birmingham CL, Goldner EM, Bakan R. Controlled trial of zinc supplementation in anorexia nervosa. Intern J Eating Disorders 1994 ; 15 : 251-5.
- Boulier A, Fricker J, Thomasset AL, Apfelbaum M. Fat free mass estimation by the two-electrode impedance method. Am J Clin Nutr 1990;52:581-5
- Bufano G, Bellini C, Cervellin G, Coscelli C. Enteral nutrition in anorexia nervosa. J Parent Ent Nutr 1990 ; 14 : 404-7.
- Casper RC, Schoeller DA, Kushner R, Hnilicka J, Gold ST. Total daily energy expenditure and activity level in anorexia nervosa. Am J Clin Nutr 1991;53:1143-50
- Chalmers J, Catalan J, Day A, Fairburn C. Anorexia nervosa presenting as morbid exercising. Lancet 1985;1:286-7
- Davis C, Fox J, Cowles M, Hastings P, Schwass K. The functional role of exercise in the development of weight and diet concerns in women. J Psychosomatic Research 1990;34:563-74
- Davis C, Kennedy SH, Ravelski E, Dionne M. The role of physical activity in the development and maintenance of eating disorders. Psychol Med 1994;6:536-9
- Dempsey DT, Crosby LO, Pertschuk MJ, Feurer ID, Buzby GP, Mullen JL. Weight gain and nutritional efficacy in anorexia nervosa. Am J Clin Nutr 1984;39:236-242
- Durnin JVGA, Womersley J. Body fat assessed from density and its estimation from skinfold thickness: measurements on 481 men and women aged from 16 to 72 years. Br J Nutr 1974;32:77-97
- Engel K, Wittern M, Hentze M, Meyer AE. Psychiatric Developments 1989 ; 7 : 395-407.
- Feighner, Robins E, Guze SE. Diagnostic criteria for use in psychiatric research. Arch Gen Psychiatry 1972 ; 26 : 57-63.
- Forbes GB, Brown MR, Welle SL, Lipinski BA. Deliberate overfeeding in men and women: energy cost and composition of the weight gain. Br J Nutr 1986;56:1-9
- Forbes GB, Kreipe RE, Lipinski BA, Hodgman CH. Body composition changes during recovery from anorexia nervosa: comparison of two dietary regimes. Am J Clin Nutr 1984;40:1137-45
- Frisancho A.R. Triceps skinfold and upper arm muscle size norms for assessment of nutritional status. Am J Clin Nutr 1974;27:1052-86 Gardner DM, Olmsted MP, Polivy J. Development and validation of a multidimensional eating disorder inventory for anorexia and boulimia. Int J Eating Dis 1983 ; 2 : 15-34.
- Hebert PC, Weingarten MA. The ethics of forced feeding in anorexia nervosa. Can Med Assoc J 1991 ; 144 : 1205-8.
- Horne M, Gallen M. Anorexia Nervosa : an object relations approach to primary treatment. Br J Psychiatry 1987 ; 151 : 192-4.
- Jeammet Ph, Brechon G, Payan Ch, Gorge A, Fermanian J. Le devenir de l'anorexie mentale : une étude prospective de 129 patients évalués au moins 4 ans après leur première admission. Psychiatrie Enfant 1991 ; 34 : 381-442.
- Kaye WH, Gwirtsman HE, Obarzanek E, George DT. Relative importance of calorie intake needed to gain weight and level of physical activity in anorexia nervosa. Am J Clin Nutr 1988;47:987-94
- Kopp HG, Ruegsegger P, Dambacher MA. Loss of bone mass in patients with anorexia nervosa on tube feeding. Schw Medizinische Wochenschrift 1992 ; 122 : 538-43.
- Kurpad AV, Kulkarni RN, Shetti PS. Reduced thermoregulatory thermogenesis in undernutrition. Eur J Clin Nutr 1989;43:27-33
- Lopes J, Russell DM, Whitwell J, Jeejeeboy KN. Skeletal muscle function in malnutrition. Am J Clin Nutr 1982;36:602-10
- Melchior JC, Rigaud D, Rozen R, Malon M, Apfelbaum M. Energy expenditure economy induced by decrease in lean body mass in anorexia nervosa. Eur J Clin Nutr 1989;43: 793-9
- Moukaddem M, Apfelbaum M, Rigaud D. Increase in diet-induced thermogenesis at the start of refeeding in severely malnourished anorexia nervosa patients. Am J Clin Nutr 1997 ; 66 : 133-40
- Murciano D, Rigaud D, Pingleton S, Armengaud MH, Melchior JC, Aubier M. Diaphragmatic function in severely malnourished patients with anorexia nervosa. Am J Respir Crit Care Med 1994;150:1569-74
- Obarzanek E, Lesem MD, Jimerson DC. Resting metabolic rate of anorexia nervosa patients during weight gain. Am J.Clin Nutr 1994 ; 60 : 666-75.
- Rigaud D, Bedig G, Merrouche M, Vulpillat M, Bonfils S, Apfelbaum M. Delayed gastric emptying in anorexia nervosa is improved by the completion of a renutrition program. Dig. Dis. Sci. 1988;33:919-25
- Rigaud D, Cohen B, Melchior JC, Moukaddem M, Reveillard V, Apfelbaum M. Refeeding improves muscle performances without normalization of muscle mass and oxygen conpsumption in anorexia nervosa. Am J Clin Nutr 1997 ; 65 : 1845-51.
- Rigaud D, Melchior JC. Le métabolisme énergétique chez l'homme. Méthodes de mesure et applications pratiques. Ed. Lavoisier (Paris); Ed Med Intern 1992;69-132
- Rigaud D, Sogni P, Hammel P, Melchior JC, Rozen R, Labarre C, Mignon M, Apfelbaum M. Anorexie mentale : absence de sensibilité des marqueurs protéiques nutritionnels ; étude de 20 malades et comparaison à un groupe apparié de maladie de Crohn colique. Ann. Med. Intern. 1989, 140 : 86-90.
- Rigaud D. Anorexie Mentale : aspect clinique et biologique. In "les conduites alimentaires". Ed. Samuel-Lajeunesse B. Ed. Masson (Paris) 1994 : 131-144.
- Russell DM, Leiter LA, Whitwell J, Marliss EB, Jeejeeboy KN. Skeletal muscle function and fasting: a comparison with standard nutritional assessment parameters. Am J Clin Nutr 1983;37:133-8
- Russell DM, Pendergast PJ, Darby PL, Garfinkel PE, Whitwell J, Jeejeebhoy KN. A comparison between muscle function and body composition in anorexia nervosa: the effect of refeeding. Am J Clin Nutr 1983;38:229-37
- Samuel-Lajeunesse B, Foulon Ch. Les conduites alimentaires. Ed. Masson (Paris) 1994 : 270 p.
- Samuel-Lajeunesse. Essai de systématisation de l'approche thérapeutique des troubles du comportement alimentaire. Ann Méd Psychol 1987 ; 145: 561-73.
- Scalfi L, Coltorti A, Borreli R, Contaldo F. Postprandial thermogenesis in leanness and anorexia nervosa. Ann Nutr Metab 1992;36:48-54
- Stordy J, Marks V, Kalucy RS, Crisp AH. Weight gain, thermic effect of glucose and resting metabolic rate during recovery from anorexia nervosa. Am J Clin Nutr 1977;30:138-46
- Vaisman N, Rossi MF, Corey M, Clarke R, Goldberg E, Pencharz PB. Effect of refeeding on the energy metabolism of adolescent girls who have anorexia nervosa. Eur J Clin Nutr 1991;45:527-37
- Vaisman N, Rossi MF, Goldberg E, Dibden LJ, Wykes LJ, Pencharz PB. Energy expenditure and body composition in patients with anorexia nervosa. J Pediatr 1988;113:919-24
- Walker J, Roberts SL, Halmi KA, Goldberg SC. Caloric requirements for weight gain in anorexia nervosa. Am J Clin Nutr 1979;32:1396-1400
Publié en 2000
